Nathalie Tessier, M.Sc., Chef de service
Nathalie.tessier.cemtl@ssss.gouv.qc.ca
(514) 252-3400 poste 3334
Dre Julie Chevrette, Vétérinaire consultante
julie.chevrette.cemtl@ssss.gouv.qc.ca
(514) 252-3400 poste 5104
Fany DeWilde, Coordonatrice de l'animalerie
(514) 252-3400 poste 5104
Marie-Ève Lebel, Coordonatrice du CPA
marie-eve.lebel.cemtl@ssss.gouv.qc.ca
Animalerie
animaleriehmr.hmr@ssss.gouv.qc.ca
(514) 252-3400 poste 3564
Hébergement souris
325 / 407 / 425 / 426 / 428A
Hébergement souris immuno-supprimées
423
Hébergement rats
424
Hébergement lapins
128
Salle de procédure souris
408
Salle imagerie in-vivo
411
| Équipements scientifiques | applications | localisation | manuel d'opération | pnf |
|---|---|---|---|---|
| Appareil d'imagerie animale in vivo | Quantification en imagerie de la fluorescence et de la bioluminescence in vivo | 411 | IVIS-Lumina-EN.pdf | M-19 Imagerie in vivo.pdf |
| Anesthésie (7x) | Suppression des sensations (douleur) visant à permettre une procédure sur des rongeurs |
| PNF M-07 : anesthésie des rongeurs | |
| Système à ultrasons | Permet l’imagerie cardiaque et vasculaire, la recherche en biologie et en cancérologie, ainsi que des techniques avancées telles que les injections guidées et l’imagerie 3D. | 408 | Prospect T1-Scintica | |
| Lampe à fente | Permet l'examen du segment antérieur et du segment postérieur de l'œil du rongeur | 410 | ZEISS VISULAS green Comfort.pdf | |
| Ophtalmoscope | Permet l'examen en image droite des milieux interne de l'œil du rongeur | 410 | Micron IV-Phoenix | |
| Stéréomicroscopes (2x) | Observation à faible grossissement d'un échantillon utilisant généralement la lumière réfléchie par la surface de ce dernier permettant d'effectuer de la dissection et/ou de la microchirurgie | 427 | Leica-M60-EN.pdf | |
| Oxycycler - A84XOV | Permet le contrôle complexe du profil d'oxygène avec plusieurs points de consigne allant de 0.1 à 99.9 % d'oxygène.
| 428A | OxyCycler-A84XOV-EN.pdf | |
| Oxycycler - PROOX P360 (2x) | Permet le contrôle fixe du profil d'oxygène avec plusieurs points de consigne allant de 0.1 à 99.9 % d'oxygène. | 428A | Oxycycler-ProOx P360-EN.pdf | |
| Électrorétinographe (ERG) | Permet l'examen électrophysiologique pour le diagnostique de certaines anomalies de la rétine | 428 | ||
| Tomographe par cohérence optique (OCT) | Procure des images en coupes très précises des couches rétiniennes permettant de détecter les signes précurseurs de maladies oculaires, notamment celles touchant la rétine et le nerf optique | 428 | OCT-Spectralis-EN.pdf |
Vous trouverez ci-bas le lien pour accéder à la plateforme Nagano CPA (Animaux).
Il est également possible d'y accéder via les applications sur tous les postes de travail du CIUSSS-EMTL à partir de l'icône ci-bas.

Approvisionnement animal
A-02 Acquisition des animaux.pdf
A-03 Importation-exportation.pdf
A-04 Réception des animaux.pdf
A-05 Acclimatation des animaux.pdf
Biorisque
B-01 Mesure à prendre en cas d'incident à l'animalerie.pdf
B-03 Désinfection de local contaminé.pdf
B-07 Mesures à prendre lors de l'utilisation d'agents cytotoxiques.pdf
B-11 Laboratoire de niveau de confinement 2 secteur animalerie.pdf
B-12 Prévention des allergies.pdf
Comité protection des animaux
C-01 Plan de gestion de crise.pdf
C-02 Visite annuelle de l'animalerie.pdf
C-03 Programme de formation.pdf
C-04 Processus de révision des protocoles et des formulaires.pdf
C-05 Soutien post-approbation.pdf
C-07 Utilisation animale hors animalerie.pdf
Manipulations animales
M-01 Accouplement et gestion de colonie.pdf
M-03 Suivi de la glycémie et induction du diabète chez les rongeurs.pdf
M-04 Observation des animaux.pdf
M-05 Prélèvements sanguins.pdf
M-10 Irradiation et soins post-irradiation.pdf
M-11 Traitements médicaux communs des rongeurs.pdf
M-12 Points limites animaux sous protocoles expérimentaux.pdf
M-21 Souris Vieillissantes.pdf
Procédures de l'animalerie
P-01 Cas clinique et suivi animal_Avril 2025.pdf
P-03 Entretien sanitaire quotidien, hebdomadaire, mensuel.pdf
P-04 Procédures laverie côté sale et utilisation du lave-cage.pdf
P-05 Procédures laverie côté propre et utilisation du stérilisateur.pdf
P-06 Identification animale.pdf
P-07 Hébergement et enrichissement du milieu.pdf
P-08 Habillement et circulation à l’intérieur de l’animalerie.pdf
P-09 Approvisionnement et entreposage de nourriture et litière.pdf
P-10 Travail sous une enceinte de sécurité biologique.pdf
P-11 Changements de cages des rongeurs.pdf
P-12 Programme de surveillance et de contrôle de la santé des rongeurs.pdf
PerDiems (Tarifs en $/cage/jour pour les souris et rats et $/animal/jour pour les autres espèces)
| Espèce | Type d'hébergement | Fonds publics | Fonds privés |
|---|---|---|---|
| Souris | Cage ventilée | 0,57 $ | 2,00 $ |
| Souris | Cage stérile | 1,14 $ | 3,81 $ |
| Souris | Quarantaine | 1,14 $ | 3,81 $ |
| Souris | Niveau de confinement 2 | 1,14 $ | 3,81 $ |
| Rat | 1,14 $ | 3,81 $ | |
| Porc | 7,59 $ | 28,69 $ | |
| Lapin | 4,03 $ | 13,33 $ |
Tâches techniques (Taux horaire : minimum 15 minutes)
| fonds publics | fonds privés |
|---|---|
| 48,96 $ | 168,30 $ |
Imagerie in-vivo (IVIS) (Taux horaire : minimum 15 minutes)
| fonds publics | fonds privés |
|---|---|
| 44,17 $ | 153,00 $ |
Frédéric Duval, Ph.D., Coordonnateur technique
frederic.duval.cemtl@ssss.gouv.qc.ca
(514) 252-3400 poste 3521 ou 6139
Anne-Marie Aubin, M.Sc., Assistante de recherche
anne-marie.aubin.cemtl@ssss.gouv.qc.ca
(514) 252-3400 poste 3521 ou 6139
INTRO
La cytométrie en flux est une technique d’analyse des caractéristiques physiques et fonctionnelles de chaque cellule au sein d’une suspension cellulaire. Ainsi, on peut évaluer les proportions de différentes sous-populations cellulaires présentes dans le milieu a très grande vitesse (plusieurs milliers de cellules par seconde). Cette technique permet une mesure précise et rapide de paramètres tels que la taille des cellules, leur nature, leur contenu en ADN ainsi que la présence de molécules spécifiques à leur surface, intracellulaires ou intranucléaires. Ces molécules sont détectées à l’aide de sondes fluorescentes qui sont excitées par des lasers.
Notre plateforme est équipée d'instruments de cytométrie spectrale et conventionnelle à la fine pointe de la technologie permettant ainsi de réponde aux exigences variées de la recherche en santé. Nous disposons de cinq analyseurs et de deux trieurs, disponibles tant en interne qu'en externe. Tous nos équipements font l'objet d'un entretien régulier, de calibrages et d'évaluations de performance pour garantir la fiabilité et la reproductibilité des données.
Les membres de notre équipe fournissent une formation approfondie aux utilisateurs, les accompagnant à chaque étape, de la conception de leurs panels de fluorochromes à l'analyse des résultats, en passant par l'optimisation des étapes clés de leur expérience.
Nos trieurs de cellules ARIA III et Cytek sont munis d'une hotte à pression négative permettant le tri d'échantillons potentiellement infectieux, y compris les cellules humaines provenant de donneurs sains. Cependant, l'approbation du comité de biosécurité est requise pour tout échantillon provenant de primates ou de cellules génétiquement modifiées non fixées.
NOTRE MISSION
Entretenir, Calibrer, évaluer la performance des instruments pour assurer l’obtention de résultats reproductibles tant au niveau de l’analyse que du tri cellulaire.
Former les usagers pour leur permettre d’atteindre leurs objectifs tant au niveau expérimental que théorique sur tous les sujets en rapport avec la cytométrie en flux (design expérimental, design de panel, acquisition, analyse, etc.).
Grace à nos appareils à spectre complet nous pouvons trier et analyser jusqu’à 40 paramètres fluorescents différents en plus d’extraire l’autofluorescence des échantillons garantissant ainsi l'obtention d’une résolution inégalée.
Analyse multiparamétrique (liste non exhaustive)
- Immunophénotypage;
- Cycle cellulaire, quantification de l’ADN et prolifération;
- Étude des espèces réactives de l'oxygène;
- Viabilité et mort cellulaire;
- Évaluation de la cytotoxicité d’une drogue ou d’un type cellulaire;
- Flux calcique;
- pH intracellulaire;
- Potentiel de la membrane cytoplasmique et mitochondriale;
- Phagocytose et autophagie;
- Autres;
Tri cellulaire à haut débit en condition aseptique
- NC2+;
- 1 à 6 populations simultanées en tubes, plaques ou sur lames;
- Cellules uniques;
- Jusqu’à 40 paramètres fluorescents;
Formation et soutien
- Acquisition sur les appareils BD Biosciences;
- Acquisition sur les appareils Cytek;
- Formations théoriques et ou pratiques personnalisables allant de la création d'expérience impliquant la cytométrie en flux à l'analyse des résultats;
Logiciels
Station d’analyse
- Équipée d’un MacBook Pro (16 pouces) 96 GB RAM;
- Deux grands écrans (>32 pouces);
- Souris sans fil;
- Adaptateur pour câble internet;
- Adaptateur pour prise USB-C/USB-A;
Trieurs
Cytek Aurora CS
Le Cytek Aurora CS est équipé de 5 lasers qui permettent la détection de 40 paramètres de fluorescence en plus des paramètres de taille (FSC) sur le laser bleu et de structure (SSC) sur les lasers bleu et violet. Cet instrument permet également d’extraire l’auto-fluorescence des cellules ce qui permet d’obtenir une meilleure résolution des signaux.
- 305 nm Ultra-Violet: 16 détecteurs de fluorescence;
- 405 nm violet : 16 détecteurs de fluorescence en plus du SSC-B;
- 488 nm bleu : 14 détecteurs en plus du SSC-A;
- 561 nm jaune-vert : 10 détecteurs de fluorescence;
- 640 nm rouge : 8 détecteurs de fluorescence
Nous utilisons des buses de différentes tailles (70 et 100uM) et des pressions différentielles variées selon le type de cellules à trier. Il est possible de trier 6 populations simultanément en tubes, en plus de faire le tri en plaque ou sur lames.
Configuration Cytek Aurora.pdf
BD ARIA III
Le BD ARIA III est équipé de 4 lasers qui permettent la détection de 16 paramètres de fluorescence en plus des paramètres de taille (FSC) et de structure (SSC).
- 407 nm violet : 6 détecteurs de fluorescence;
- 488 nm bleu : 3 détecteurs (SSC et 2 détecteurs de fluorescence);
- 561 nm jaune-vert : 5 détecteurs de fluorescence;
- 633 nm rouge : 3 détecteurs de fluorescence
On utilise des buses de différentes tailles (70, 85 et 100 µm) et des pressions différentielles variées selon le type de cellules à trier. Il est possible de trier 4 populations simultanément, en plus de faire le tri en plaque.
Configuration Trieur BD Aria III.pdf
Analyseurs
Cytek Aurora
Le Cytek Aurora est équipé de 5 lasers qui permettent la détection de 40 paramètres de fluorescence en plus des paramètres de taille (FSC) sur le laser bleu et de structure (SSC) sur les lasers bleu et violet. Cet instrument permet également d’extraire l’auto-fluorescence des cellules ce qui permet d’obtenir une meilleure résolution des signaux.
- 305 nm Ultra-Violet: 16 détecteurs de fluorescence;
- 405 nm violet : 16 détecteurs de fluorescence en plus du SSC-B;
- 488 nm bleu : 14 détecteurs en plus du SSC-A;
- 561 nm jaune-vert : 10 détecteurs de fluorescence;
- 640 nm rouge : 8 détecteurs de fluorescence;
Configuration Cytek Aurora.pdf
BD LSR Fortessa X-20 (x2)

Les 2 BD LSRFortessa X-20 sont équipés de 5 lasers qui permettent la détection de 16 paramètres de fluorescence en plus des paramètres de taille (FSC) et de structure (SSC). L’un d’entre eux est équipé d’un lecteur de plaque HTS.
- 355 nm Ultra-Violet : 3 détecteurs de fluorescence;
- 405 nm violet : 6 détecteurs de fluorescence;
- 488 nm bleu : 3 détecteurs (SSC et 2 détecteurs de fluorescence);
- 561 nm jaune-vert : 4 détecteurs de fluorescence;
- 633 nm rouge : 3 détecteurs de fluorescence
Configuration 2 BD LSRFortessa X20.pdf
BD FACSCelesta
Le BD FACSCelesta est équipé de 3 lasers qui permettent la détection de 12 paramètres de fluorescence en plus des paramètres de taille (FSC) et de structure (SSC).
- 405 nm violet : 5 détecteurs de fluorescence;
- 488 nm bleu : 5 détecteurs (SSC et 4 détecteurs de fluorescence);
- 633 nm rouge : 3 détecteurs de fluorescence
Il est possible de changer les filtres et les miroirs sur cet instrument, afin de détecter différentes combinaisons de fluorochromes.
Configurations BD FACSCelesta.pdf
BD LSRI
Le BD LSR II est équipé de 4 lasers qui permettent la détection de 10 paramètres de fluorescence en plus des paramètres de taille (FSC) et de structure (SSC).
- 355 nm Ultra-Violet : 2 détecteurs de fluorescence;
- 407 nm violet : 2 détecteurs de fluorescence;
- 488 nm bleu : 5 détecteurs (SSC et 4 détecteurs de fluorescence);
- 633 nm rouge : 2 détecteurs de fluorescence
Il est également possible de changer les filtres et les miroirs sur cet instrument, afin de détecter différentes combinaisons de fluorochromes.
Configurations BD LSRII.pdf
- Avant d'accéder aux équipements de la plateforme, tous les utilisateurs doivent suivre une formation dispensée par un membre de l'équipe de la plateforme. Les utilisateurs ne sont pas autorisés à former de nouveaux utilisateurs. En plus d’offrir un support continu allant de la conception expérimentale à l'analyse des données, la plateforme propose deux types de formations :
- Utilisation des Analyseurs BD (BD LSRII; BD FACSCelesta; BD LSRFortessa X-20);
- Utilisation de l'Analyseur Cytek Aurora.
- Chaque utilisateur doit réserver l'instrument de son choix ainsi que la plage horaire qui lui convient via le logiciel Midas. Après chaque utilisation, il est de la responsabilité de l'utilisateur de mettre à jour sur Midas le temps réellement utilisé sur l'instrument. La facturation de tous les équipements de la plateforme est basée sur les réservations effectuées sur Midas. Un tutoriel est disponible sur l’intranet dans Enseignement, recherche et innovation, Recherche, Infrastructures, Réservations.
- Si un utilisateur ayant réservé se présente alors que vous utilisez encore l'instrument, il vous sera demandé de libérer immédiatement l'instrument pour lui permettre de commencer son travail.
- Il est de votre responsabilité de contacter la personne réservée après vous si vous terminer plus tôt que ce que vous aviez prévu et réservé sur Midas.
- Les réservations excessives ne sont pas autorisées.
- L'utilisateur est responsable d'éteindre le cytomètre s'il est le dernier à l'utiliser.
- Si le dernier utilisateur doit annuler sa réservation, il doit contacter la plateforme pour demander l'extinction de l'instrument ou venir l'éteindre lui-même. Aucun instrument ne peut rester allumé la nuit ou le week-end.
- Après chaque utilisation, les fichiers FCS enregistrés doivent être supprimés du logiciel d'acquisition (DIVA ou SpectroFlo) et du disque dur de l'ordinateur. Il est recommandé d'exporter les expériences sur un disque dur externe si une réutilisation de cette expérience est envisagée.
- La plateforme de cytométrie n'est pas responsable du stockage des données. L’utilisateur est le seul responsable de ses données. La plateforme se réserve le droit de supprimer toutes les données sans préavis.
- Aucun logiciel ne doit être installé sur les ordinateurs de la plateforme sans l'autorisation des coordonnateurs.
- Il est impératif de reconnaître la plateforme dans toute publication utilisant des données de cytométrie et de lui envoyer une copie de l'article.
- Un support continu est offert par les coordonnateurs de la plateforme, du design expérimental à l’analyse des données de cytométrie ainsi que des formations spécifiques sur demande.
Formulaire de tri potentiellement infectieux F-28
- À remplir sur le logiciel Nagano
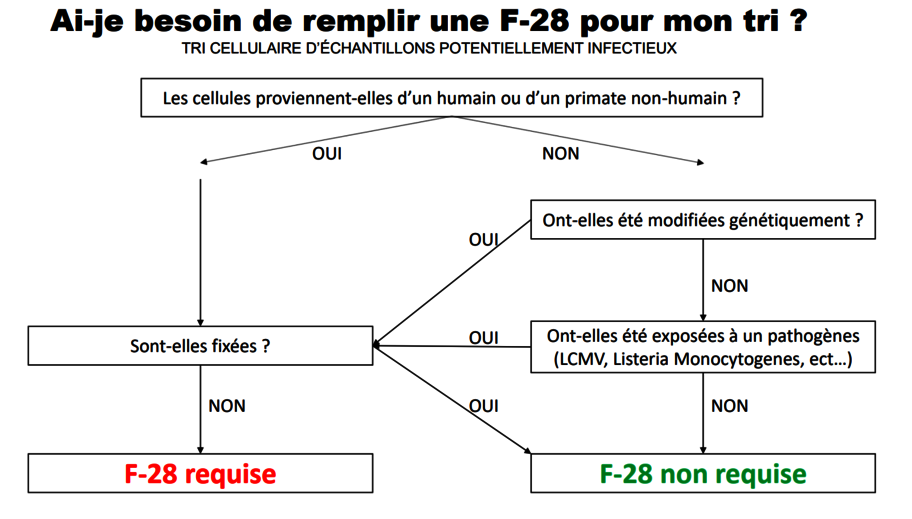
Formulaire d’aide au tri
| Équipements | Sans assistance | Avec assistance | Externe académique | Industrie |
|---|---|---|---|---|
| Celesta | 27,86 $ | 55,73 $ | 78,02 $ | 167,19 $ |
| CYTEK Analyseur | 27,86 $ | 55,73 $ | 78,02 $ | 167,19 $ |
| LSRII | 27,86 $ | 55,73 $ | 78,02 $ | 167,19 $ |
| Fortessa | 27,86 $ | 55,73 $ | 78,02 $ | 167,19 $ |
| Formation | 47,93 $ | 133,76 | 261,38 | |
| Tri cellulaire Cytek | 43,05 $ | 74,67 $ | 194,75 $ | 290,08 $ |
| Tri cellulaire ARIA | 43,05 $ | 74,67 $ | 194,75 $ | 290,08 $ |
| FlowJo | 10,25 $ / jour | 30,75 $ / jour | ||
| CellEngine | 30,75 $ / jour | 51,25 $ / jour | ||
| Station d'analyse | 10,25 $ / jour | 30,75 $ / jour |
Taux horaire: minimum 15 minutes
Mikhail Sergeev, Ph.D.
(514) 252-3400 poste 5095
INTRO
Le flux de travail typique pour la bioimagerie est la suivante:
Un étudiant, post-doc et/ou assistant de recherche me contacte.
Nous discutons des détails du projet :
- contexte scientifique
- question biologique
Nous discutons des équipements les plus adaptés :
- les bio-essais et les instruments de microscopie correspondants
- réactifs (lignées cellulaires, plasmides, méthodes de transduction, biomarqueurs, matériel de microscopie, etc.)
Formation
- session initiale (peut être un petit groupe)
- formation individuelle
- formation de suivi
Nous discutons des stratégies d'analyse des images.
La plate-forme de bioimagerie met à la disposition des chercheurs du CRHMR des équipements de pointe en microscopie optique, formations en microscopie et le soutien dans le développement d'expériences de microscopie à venir.
Liste des appareils - Bioimagerie_FR.pdf
La plateforme est également équipée d’un ophtalmoscope à balayage laser Heidelberg modèle HRA2 pour des applications d’imagerie de la rétine sur des animaux vivants. Cet instrument permet une exploration fonctionnelle de la vision in vivo. Pour plus de détails, veuillez vous référer à la liste des équipements sous la section « Animalerie ».
| Équipement | Station | Sans assistance | Avec assistance | Externe académique | Industries |
|---|---|---|---|---|---|
| Confocal | 1 | 35,66 $ | 63,70 $ | 117,03 $ | 200,63 $ |
| 2 Photons | 13 | 35,66 $ | 63,70 $ | 117,03 $ | 200,63 $ |
| Laser scanning microscope | 2 | 14,48 $ | 25,08 $ | 55,73 $ | 100,32 $ |
| Microscope avec imagerie | |||||
Deltavision | 3 | 14,48 $ | 25,08 $ | 55,73 $ | 100,32 $ |
Z1 live cell | 4 et 6 | 14,48 $ | 25,08 $ | 55,73 $ | 100,32 $ |
Z2 | 5 | 14,48 $ | 25,08 $ | 55,73 $ | 100,32 $ |
| Formation | 63,55 $ | 172,76 $ | 334,39 $ | ||
| Microscopie over night | 48,83 $ | NA | NA | NA | |
| Microscope à haut débit | 35,66 $ | 63,70 $ | 117,03 $ | 200,63 $ | |
| Microscope super-résolution | 35,66 $ | 63,70 $ | 117,03 $ | 200,63 $ | |
| Incucyte par chambre | 0,38 $ | 0,67 $ | 1,50 $ | 2,70 $ |
Taux horaire: minimum 15 minutes
La banque de cellules leucémiques du Québec (BLCQ) est un programme provincial financé par le Réseau de la recherche sur le cancer du Fonds de recherche en Santé du Québec (FRSQ). Il regroupe des hématologues, des chercheurs et des scientifiques cliniciens de quatre universités québécoises (Université Laval, McGill, Sherbrooke, Montréal) et de l’ensemble des centres de recherche du Québec.
Coordonnateur
François Béliveau, 514 252-3400, poste 4678
bclq@ssss.gouv.qc.ca
Services
Analyse et mise en banque de spécimens de cancers hématologiques
La BCLQ constitue une banque de cellules humaines de néoplasies hématologiques bien caractérisées. L’ADN constitutionnel est conservé pour chaque spécimen et une banque de données informatisées recense toutes les analyses de laboratoire effectuées sur les spécimens ainsi que les données cliniques correspondantes.



